「 モデルナのワクチンが承認されれば、ファイザー社製との混乱を避けるため、自治体の接種会場ではなく、国が、東京と大阪に開設する大規模な会場で使用されるという見通しを示しました。」
と報道されました。
日本国内においては、ワクチン接種の遅延が言われています。
筆者が地方にいて感じることは、とにかくワクチンが来ない。そしてやっと来たといっても、国からは突然配布され、ワクチンが実際に来たのを確認して、そこから自治体は接種予定者に連絡します。接種券は郵送で送り、被接種者は具体的な希望する接種可能な医療機関に、電話して接種予約を取ります。医療機関側は、6の倍数で予約人数を密にならないよう、日常診療に過度に負担にならないよう気を配って予約を受けます。等々です。
これらが今のスキームでは相応に時間がかかります。
ワクチン接種遅延の責任を我々医療者側に押し付けられても困ります。
なおこの中でびっくりしたのは、キャンセルがあったときは、そのワクチンを廃棄してくれと自治体から言われたことです。常にスマホを持っていてキャンセル待ちできるお年寄りがどれだけいるでしょう。廃棄するぐらいならだれにでも打ってあげた方がいいと思うのは、筆者だけでしょうか。
オリンピック時の看護師派遣の問題もあります。筆者は、もともとオリンピック開催は支持してきましたが、この医療崩壊を起こしている今日にもかかわらず、医療者を何百人もオリンピックに持っていくというのは、あまりにも理不尽です。国民の理解を得られるはずがありません。
開催が必要であるなら、政治家たちは、既成事実的な発言はせず、国民に丁寧に説明をすべきでしょう。
今、橋下氏がテレビで言っておられたように、オリンピックを開催するかどうかの判断を、しかるべき期日にどういう状況なら中止するということを、国民にアナウンスしておくべきだと思います。そうでないと国民は全く協力しないでしょうし、強引に開催すれば、これからのコロナ対策にも大きな悪影響を及ぼすことでしょう。
当たり前のことですが、政治家たちは、国民の気持ちに真摯に向き合わなければいけません。
今日は、こんな愚痴から書いてしまいましたが、本当はこれから大都市で行われる大規模接種を控え、モデルナワクチンに関して、現時点での知見のまとめを記事にしておきたいと思います。
以上、筆者も過去に記事を書かせていただきました。
1)
原著
mRNA-1273SARS-CoV-2ワクチンの有効性と安全性
2021年2月4日
NEngl J Med 2021; 384:403-416
DOI:10.1056 / NEJMoa2035389
バックグラウンド
mRNA-1273ワクチン(モデルナワクチン)は、Covid-19を引き起こすウイルスである重症急性呼吸器症候群コロナウイルス2(SARS-CoV-2)の融合前安定化完全長スパイクタンパク質をコードする脂質ナノ粒子カプセル化mRNAベースのワクチンです。
メソッド
この第3相ランダム化、オブザーバー盲検、プラセボ対照試験は、全米の99のセンターで実施されました。SARS-CoV-2感染またはその合併症のリスクが高い人は、1:1の比率でランダムに割り当てられ、28日間隔でmRNA-1273(100μg)またはプラセボの筋肉内注射を2回受けました。
結果
この試験には、ワクチンまたはプラセボのいずれかを受け取るために1:1の比率でランダムに割り当てられた30,420人のボランティアが登録されました(各グループに15,210人の参加者)。参加者の96%以上が両方の注射を受け、2.2%がベースラインでSARS-CoV-2感染の証拠(血清学的、ウイルス学的、または両方)を持っていました。症候性のCovid-19疾患は、プラセボグループの185人の参加者(1000人年あたり56.5; 95%信頼区間[CI]、48.7〜65.3)およびmRNA-1273グループの11人の参加者(1000人あたり3.3-年; 95%CI、1.7から6.0); ワクチン有効性は94.1%(95%CI、89.3〜96.8%; P <0.001)でした。重度のCovid-19は30人の参加者で発生し、1人が死亡しました。30人全員がプラセボグループに属していました。ワクチン接種後の中程度の一過性の副反応は、mRNA-1273グループでより頻繁に発生しました。重篤な有害事象はまれであり、発生率は2つのグループで類似していた。
結論
mRNA-1273ワクチンは、重度の疾患を含むCovid-19の病気の予防に94.1%の有効性を示しました。一過性の局所および全身反応を除いて、安全上の懸念は確認されませんでした。
2)
原著
高齢者におけるSARS-CoV-2mRNA-1273ワクチンの安全性と免疫原性
2020年12月17日
NEngl J Med 2020; 383:2427-2438
DOI:10.1056 / NEJMoa2028436
メソッド
年齢(56〜70歳または71歳以上)に応じて層別化された40人の高齢者を含むように拡大されました。すべての参加者は、28日間隔で投与される25μgまたは100μgのワクチンの2回の投与を受けるように順番に割り当てられました。
結論
高齢者を対象としたこの小規模な研究では、mRNA-1273ワクチンに関連する有害事象は主に軽度または中等度でした。100μgの用量は、25μgの用量よりも高い結合および中和抗体力価を誘導しました。これは、第3相ワクチン試験での100μgの用量の使用をサポートします。
結合-抗体反応
S-2Pおよび受容体結合ドメインへのIgG抗体の幾何平均力価(GMT)の結合は最初のワクチン接種後に急速に増加しました。
T細胞応答
S特異的ペプチドプールに応答して、ワクチンは、100μgの用量を投与された2つの年齢サブグループの参加者および56歳から70歳の参加者の間で1型ヘルパーT(Th1)細胞を含む強いCD4サイトカイン応答を誘発しました。
液性免疫も細胞性免疫もワクチン接種後にちゃんと増加するようです。
3)
mRNA-1273ワクチンによって誘発される血清中和活性
2021年4月15日
NEngl J Med 2021; 384:
1468-1470 DOI:10.1056 / NEJMc2102179
mRNA-1273ワクチン接種者から採取された血清の各種変異株に対する中和活性のデータを発表しました。
測定対象は,武漢で当初分離されたWuhan-Hu-1 (以下,武漢株),D614G変異株,英国由来B.1.1.7株, 南アフリア由来B.1.351株, ブラジル由来P.1株, 米国カリフォリニア由来B.1.427/B.1.429株, (B.1.1.7+E484K)株, その他の変異株 (20E [EU1], 20A.EU2, N439K-D614G, およびデンマークで最初に分離されたミンククラスター5)です。
P.1変異株,B.1.427/B.1.429変異株,B.1.1.7+E484K変異株,およびB.1.351変異株に対しては中和活性低下が見られました。中和抗体価で見ると,低下度合いは,2.3分の1からB.1.351株の6.4分の1までに分布しました。
それぞれの変異株に対するmRNA-1273ワクチンの有効性の検証は今後の課題です。
これは、in vitro のデータです。臨床での有効性のデータが必要です。
次にCDCのホームページよりモデルナワクチンについて、
3)
CDC
ModernaCOVID-19ワクチンの概要と安全性
2021年4月5日更新
一般情報
名前: mRNA-1273
メーカー: ModernaTX、Inc。
ワクチンの種類: mRNA
ショット数: 2ショット、1か月(28日)間隔
成分および添加物
mRNA-1273ワクチンの脂質壁は、次の4つの異なる化合物で構成されています。
① SM-102 —ナノ粒子壁の基本構造を構成する独自のリン脂質
② DSPC —ナノ粒子の壁構造を助ける別の市販のリン脂質
③ コレステロール—私たちのすべての細胞膜に固有のコレステロールは、温度に応じて細胞膜に流動性または剛性を追加するのに役立ちます。コレステロールの添加は、ナノ粒子の安定性を助けます。
④ PEG-2000 DMG —ナノ粒子の形成を助けるポリエチレングリコールに融合した脂質
mRNA
モデルナのワクチンのmRNA成分は、免疫応答を誘発する特定のコロナウイルス抗原のコピーを生成するための青写真を人体に提供します。
mRNAは、プラスミドと呼ばれるループ構造に組み込まれたDNAテンプレートを使用してラボで生成されます。プラスミドは細菌ゲノムに由来し、現在、遺伝子をシャトルまたはクローン化するために使用される一般的なバイオテクノロジーツールです。DNAテンプレートは、パンデミックの発生時に中国の武漢で分離されたSARS-CoV-2ウイルスに由来します。
追加の成分
ナノ粒子の製造に使用される化合物以外にも、ワクチンが送達される水性環境を制御するために使用されるいくつかの成分があります。これらには次のものが含まれます。
① トリス緩衝液—トリスアミノメタン(Tris)は、溶液のpH変動から保護するために、生物学的化合物で一般的に使用される緩衝液です。
② ショ糖—ラボグレードのテーブルシュガーはナノ粒子の温度安定性を高めます
③ 酢酸ナトリウム—酢に非常によく似た化合物で、粒子の安定化に役立ちます。
ファイザー社製ワクチンとは若干異なりますが、やはり PEG-2000 が気になります。
4)
Covid-19のmRNA-1273ワクチンの2回目の投与後6か月までの抗体の持続性
2021年4月6日
DOI:10.1056 / NEJMc2103916
第1相臨床試験における33人の健康な成人の参加者にmRNA1273誘発結合および中和抗体を記述2-4年齢に応じて層別化し、180日100μgの(日209)の第二の用量の後で、抗体活性は209日目ですべての年齢層で高いままでした。mRNA-1273によって誘発された抗体は2回目の投与後6か月間持続しました。進行中の研究では、6か月を超えて免疫応答を監視し、ブースター用量の効果を決定して、新たなウイルス変異体に対する活動の期間と幅を拡大しています。
5)
この筆者の記事の中で、モデルナ社製ワクチンの副反応について記載しています。
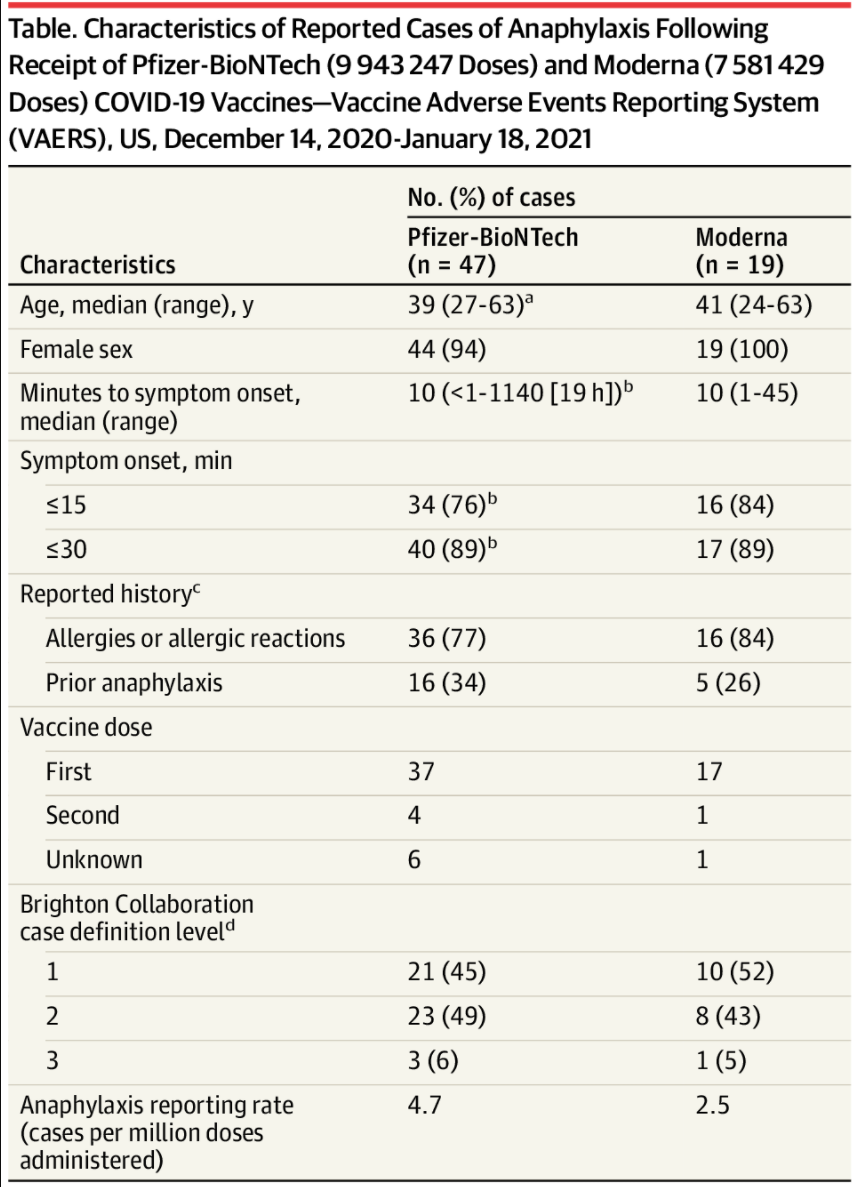
この時点でモデルナワクチンのアナフィラキシーは、すべて女性で、45分以内に出現しています。
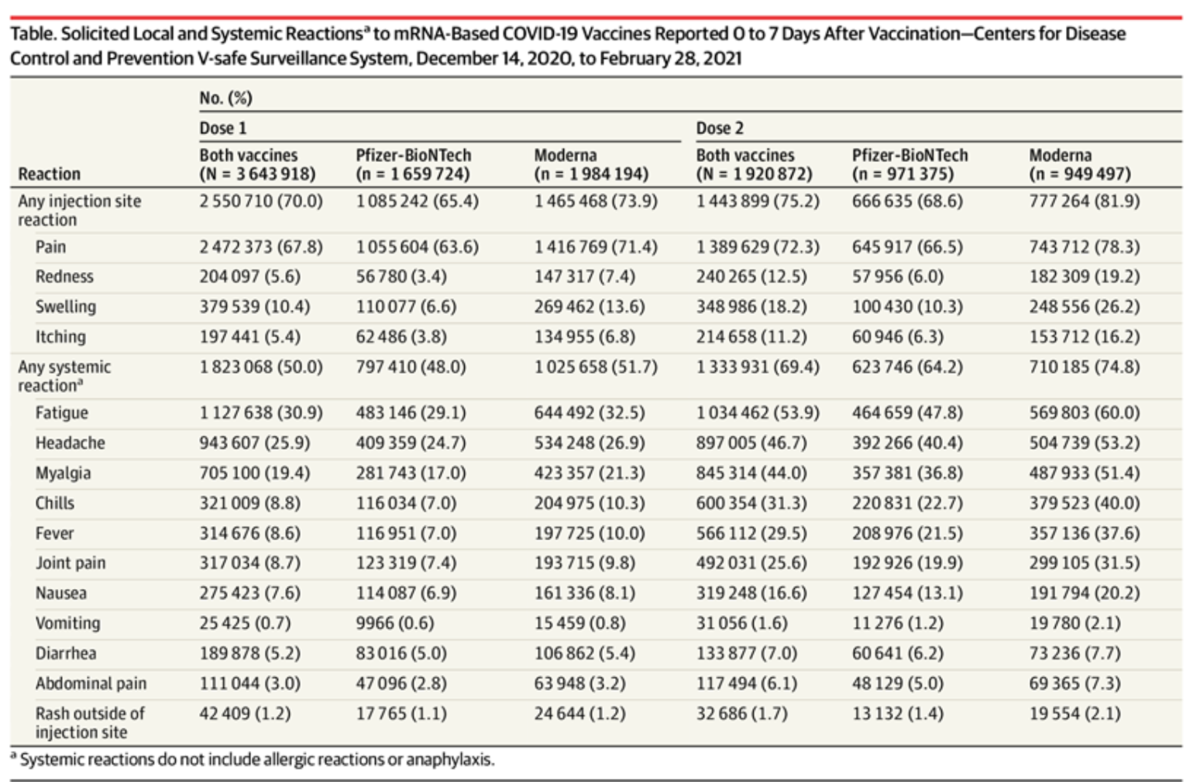
JAMAインサイト
2021年4月 5日
mRNAベースのCOVID-19ワクチンの受領後の反応原性
https://jamanetwork.com/journals/jama/fullarticle/2778441
上記は、 C D C のその後のデータです。サンプルサイズがかなり増えています。
これには、アナフィラキシーは、含まれていません。ファイザー社製ワクチンよりモデルナ製ワクチンのほうが、一回目より二回目のほうが、副反応は多くなっています。
CDC
Moderna COVID-19ワクチンの初回投与を受けた後のアナフィラキシーを含むアレルギー反応—米国、2020年12月21日〜2021年1月10日
報告されたModerna COVID-19ワクチンの初回投与が米国で4,041,396回投与され、Moderna COVID-19ワクチンの受領後の1,266(0.03%)の有害事象の報告がイベント報告システム(VAERSワクチン有害事象)に提出されました。これらの中で、アナフィラキシーを含む重度のアレルギー反応の可能性のある症例として、108の症例報告がさらなるレビューのために特定されました。
(投与されたModerna COVID-19ワクチン投与量100万回あたり2.5アナフィラキシー症例の割合です。)
これは、副反応と違ってファイザー社製ワクチンより少ない値です。
今日は、今後日本で接種が予定されている Mderna 社製ワクチンについて論文やニュース、レポートをもとに書かせていただきました。副反応などで若干ファイザー社製ワクチンと異なりますが、同じmRNA ワクチンで有効率は非常に高いです。
一日も早くワクチン接種が進むことを祈っています。
今回も最後までお付き合いいただきまして、誠にありがとうございました。